Lääkinnällisen laitteen turvallisuusilmoitus
Philips Respironicsin uniapnea- ja hengityshoitolaitteet
FSN 2021-05-A ja FSN 2021-06-A
Lokakuusta 2023 alkaen Philips Respironics on aloittanut Trilogy 100/200 -laitteiden korjaustoiminnan Philipsin hyväksymien korjauskeskusten kautta useissa maissa.
Asiakkailla on edelleen mahdollisuus valita laitteidensa korjauksen, Trilogy Evo myyntihyvityksen ja Trilogy Evo -lainausohjelman välillä. Tavoitteemme on yhteistyössä asiakkaiden kanssa mahdollisimman pian suorittaa korjaavat toimenpiteet Trilogy 100/200 laitteille, jotka ovat potilaskäytössä.
Ota yhteyttä Philips Respironics -asiakaspäällikköön, jos sinulla on kysyttävää.
Alla on päivitys vaurioituneiden CPAP-, BiPAP- ja mekaanisten hengityslaitteiden korjaus- ja vaihto-ohjelmamme tilasta 31. lokakuuta 2024. Toimitettujen vaihtolaitteiden määrän lisäksi tarjoamme myös yleiskatsauksen niiden laitteiden määrästä, jotka korvataan taloudellisesti ja niiden laitteiden määrästä, joita kotihoidon tarjoajat eivät enää pysty jäljittämään.
1,037,268
Länsi-Eurooppaan valmistettujen korjaussarjojen ja vaihtolaitteiden määrä
3,793
Asiakkaille Suomessa toimitettujen korjattujen laitteiden määrä
4,499
Taloudellinen korvaus1 laitteista kotihoidon tarjoajille
344
Jäljittämättömät laitteet2
1. Philips ei enää valmista ja myy useita vanhempia System One -uniapnealaitteita. Usein nämä laitteet ovat yli viisi vuotta vanhempia. Philips on neuvotellut kotihoidon tarjoajien kanssa ratkaisusta näitä potilaita varten. Osalle käytetyistä laitteista kotihoidon tarjoajat saavat vaihtoehtoisia tai korjattuja laitteita. Lisäksi Philips tarjoaa rahallista korvausta joistakin näistä System One -laitteista, jotta kotihoidon tarjoajat voivat ostaa toisen laitteen potilaalle.
2. Kotihoidon tarjoajat ovat rekisteröineet useita laitteita, jotka eivät ole enää käytössä tai joita ei voida enää jäljittää. Kotihoidon tarjoajat ovat pyrkineet jäljittämään kaikki laitteet ja potilaat. Oletamme, että laitteet, joita ei enää voida jäljittää, eivät ole enää käytössä.
You are about to visit a Philips global content page
Continue
Kesäkuussa 2021 havaittuaan mahdollisen terveysriskin, joka liittyy vaahtoon tietyissä CPAP-, BiPAP- ja Mechanical Ventilator -laitteissa, Philips Respironics julkaisi vapaaehtoisen kenttäturvallisuusilmoituksen.
Keskitymme tarjoamaan parasta mahdollista hoitoa samalla kun tuemme potilaita, asiakkaita ja lääkäreitä koko hoitoprosessin ajan.
Viimeisimmät päivitykset
Philips antaa päivityksen Respironicsin turvallisuusilmoituksesta
lokakuuta 06, 2023
Philipsin vastaus viimeaikaisiin tiedotusvälineiden artikkeleihin, jotka liittyvät Philips Respironicsin vapaaehtoiseen turvallisuusilmoitukseen
syyskuuta 27, 2023
Heinäkuun 2023 viimeisimmät tulokset ja johtopäätökset unihoitolaitteista otsonipuhdistuksen vaikutuksesta eivät osoita merkittävää haittaa potilaiden terveydelle
Philips Respironics suoritti System One- ja DreamStation Go -uniterapialaitteiden analyysit, jotka osoittivat, että vaahdon hajoamiseen liittyvät haihtuvat orgaaniset yhdisteet (VOC) ja hiukkaspäästöt (PM) ovat sovellettavien turvallisuusrajojen sisällä. Muita visuaalisia arviointeja on tehty ja ne vahvistavat vaahdon merkittävän hajoamisen vähäisen esiintyvyyden.
You are about to visit a Philips global content page
Continue

Puhdistukseen käytettävät otsonilaitteet ja UV-valolaitteet eivät ole tällä hetkellä uniapnealaitteiden tai maskien hyväksyttyjä puhdistusmenetelmiä, eikä niitä saa käyttää.
Etkö ole rekisteröitynyt?
Kysymyksiä ja vastauksia
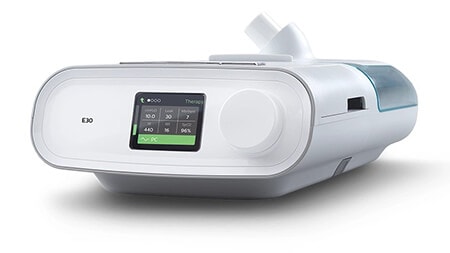
E30
(Käyttö sallittu hätätilanteessa, Emergency Use Authorization)

DreamStation ASV
Toiselta nimeltään DreamStation BiPAP autoSV

DreamStation ST, AVAPS
Toiselta nimeltään DreamStation BiPAP AVAPS, DreamStation BiPAP S/T

SystemOne ASV4
Toiselta nimeltään System One BiPAP autoSV, System One BiPAP autoSV Advanced

C-sarjan ST, AVAPS
Toiselta nimeltään One BiPAP AVAPS (C-sarja), System One BiPAP S/T (C-sarja)

OmniLab Advanced Plus
Titrauslaite laboratoriokäyttöön

System One 50 -sarja
CPAP-laitteet, Auto CPAP, BiPAP-laitteet

System One 60 -sarja
CPAP-laitteet, Auto CPAP, BiPAP-laitteet

DreamStation CPAP, Auto CPAP, BiPAP

DreamStation GO CPAP, APAP, Auto CPAP

Dorma 400, 500 CPAP, Auto CPAP
(ei markkinoida Yhdysvalloissa)
Jos asia koskee laitettasi...
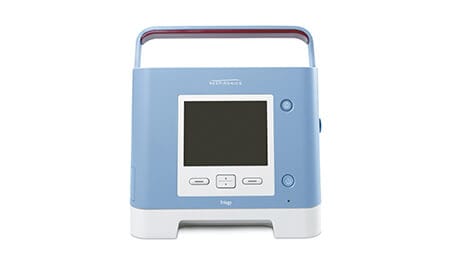
Trilogy 100 -ventilaattori

Trilogy 200 -ventilaattori

Garbin Plus-, Aeris-, LifeVent-ventilaattori
(ei markkinoida Yhdysvalloissa)
Jatkuvakäyttöinen ventilaattori, lievä hengitystuki, laitoskäyttö

A-sarjan BiPAP Hybrid A30
Toiselta nimeltään BiPAP Hybrid A30 -ventilaattori (A-sarja)
(ei markkinoida Yhdysvalloissa)

A-sarjan BiPAP V30 Auto -ventilaattori
Toiselta nimeltään BiPAP V30 Auto -ventilaattori (A-sarja)
Jatkuvakäyttöinen ventilaattori, ei elintoimintoja ylläpitävä

A-sarjan BiPAP A40
Toiselta nimeltään BiPAP A40 -ventilaattori (A-sarja)
(ei markkinoida Yhdysvalloissa)

A-sarjan BiPAP A30
Toiselta nimeltään BiPAP A30 -ventilaattori (A-sarja)
(ei markkinoida Yhdysvalloissa)
Jos asia koskee laitettasi...
Mitkä tuotteet eivät ole muutostyön alaisia ja miksi?
Tuotteissa, jotka eivät ole muutostyön alaisia, on ehkä käytetty jotain muuta äänenvaimennusmateriaalia, sillä ajan myötä saataville on tullut uusia materiaaleja ja tekniikoita. Tuotteissa, jotka eivät ole muutostyön alaisia, äänenvaimennusmateriaali on saatettu sijoittaa laitteessa eri kohtaan.




